Parkinson ist eine neurodegenerative Erkrankung, die bei Menschen über 60 Jahren häufiger auftritt – ihre Verbreitung wird in den alternden westlichen Gesellschaften deshalb aller Voraussicht nach zunehmen. Was passiert im Gehirn der Erkrankten? Wie wird Parkinson diagnostiziert und behandelt? Und was ist der Stand der Forschung?
- Wie viele Menschen leiden in Südtirol an der Parkinson-Krankheit?
- Wer ist besonders betroffen?
- Berühmte Parkinson-Kranke
- Warum erkrankt man?
- Schützt Rauchen vor Parkinson?
- Gibt es Umweltfaktoren, deren Schädlichkeit als erwiesen gilt?
- Was passiert im Gehirn von Parkinson-Kranken?
- Stirbt man an Parkinson?
- Der Tremor ist das bekannteste Symptom. Was sind andere häufige Symptome?
- Ist Parkinson heilbar?
- Gibt es eine Impfung?
- Wie weit entfernt ist man davon, die Erkrankung heilen zu können?
- Was könnte einen Durchbruch in der Diagnose bedeuten?
- Molekulare Forschung bei Eurac Research
- Meilensteine der Parkinson-Forschung
- Wie viele öffentliche und private Mittel fließen in die Parkinson-Forschung?
- Was sind die wichtigsten Anlaufstellen für Kranke in Südtirol?
Contents
Das [Dossier Parkinson] als PDF-Download
Wie viele Menschen leiden in Südtirol an der Parkinson-Krankheit?
Etwa 1.500. Dies entspricht den internationalen Zahlen: Von tausend Menschen erkranken zwei bis drei an Parkinson, das sind etwa 0,3 Prozent der Bevölkerung. Die Häufigkeit nimmt mit dem Alter zu: Bei Menschen über 60 liegt die Wahrscheinlichkeit, an Parkinson zu erkranken, bei etwa einem Prozent, auch in Südtirol. Da die Menschen immer älter werden, geht man in der Medizin davon aus, dass auch die Krankheit in Zukunft häufiger auftreten wird. Von den 13.000 Menschen, die an der ersten Phase der Gesundheitsstudie CHRIS von Eurac Research und dem Südtiroler Sanitätsbetrieb teilgenommen haben, waren etwa 20 von der Parkinson-Krankheit betroffen, was der generellen Häufigkeit entspricht.
Personen über 60, die an Parkinson erkranken
1 von 100
Wer ist besonders betroffen?
Männer erkranken etwa doppelt so häufig wie Frauen. Das Erkrankungsrisiko verschiedener Bevölkerungen unterscheidet sich im Allgemeinen nicht; nur in einigen sehr abgeschlossenen Populationen kommen familiäre Formen der Krankheit vermehrt vor. So ist die Inzidenz, das heißt die Häufigkeit von Neuerkrankungen in einem Jahr, zum Beispiel bei aschkenasischen Juden in den USA oder bei Berbern in Nordafrika außergewöhnlich hoch. In Südtirol betrifft die Erkrankung Männer etwas häufiger als Frauen.
Männer erkranken etwa doppelt so häufig wie Frauen.
Warum erkrankt man?
Die Ursachen der Krankheit sind noch nicht bekannt. Mehrere Faktoren spielen aber bei der Entstehung eine Rolle, darunter genetische Veranlagung und Umwelteinflüsse. Dank der genetischen Untersuchungen der vergangenen 20 Jahre kann man heute zehn Prozent der Parkinson-Fälle auf eine bestimmte Mutation oder Genveränderung zurückführen, es handelt sich in diesen Fällen also um eine erbliche Form der Krankheit. Bisher wurden etwa 20 Gene entdeckt, die mit der Entstehung der Krankheit in Zusammenhang stehen.
In einem von zehn Fällen hat die Krankheit genetische Ursachen.
Genforschung: Parkinson in Südtirol
Um die genetischen Ursachen der Parkinson-Krankheit zu erforschen, werden Familien mit mehreren Betroffenen über mehrere Generationen hinweg untersucht. Die Forscher rekonstruieren den Stammbaum – im Idealfall über drei oder vier Generationen – und vergleichen DNA und Merkmale möglichst vieler Familienmitglieder. Ziel ist, herauszufinden, welche genetische Mutation die erkrankten von den gesunden Familienmitgliedern unterscheidet. Das Forschungsteam von Eurac Research hat bei seinen Untersuchungen Stammbäume erstellt mit mehreren von Parkinson betroffenen Mitgliedern, die Träger einer Mutation im Parkin-Gen sind. Wer eine Mutation in diesem Gen sowohl von seinem Vater als auch von seiner Mutter erbt, wird mit hoher Wahrscheinlichkeit erkranken, und zwar meist an einer frühzeitig – häufig schon vor dem 45. Lebensjahr – auftretenden Form der Krankheit. Glücklicherweise ist dies jedoch selten. Häufiger wird eine Mutation nur von einem Elternteil vererbt (heterozygote Mutationen): In diesen Fällen ist die Wahrscheinlichkeit, dass die Betroffenen erkranken, sehr gering; wenn die Krankheit aufritt, dann meist erst in fortgeschrittenem Alter und mit leichteren Symptomen. Die CHRIS-Studie ermöglicht den Forschern, weitere Träger von heterozygoten Mutationen des Parkin-Gens zu identifizieren und zu untersuchen, warum bei einigen Mutationsträgern subklinische (sehr milde) Symptome auftreten, und bei anderen nicht. Erforscht werden dabei insbesondere Variationen in der – von der Mutter vererbten – mitochondrialen DNA, also in den Energiezentren unserer Zellen.
Schützt Rauchen vor Parkinson?
Epidemiologische Studien haben einen Zusammenhang zwischen dem Konsum von Nikotin, aber auch von Koffein, und einer geringeren Inzidenz von Parkinson gezeigt. Solche Studien bilden eine bestimmte Situation ab und analysieren das erhaltene Bild statistisch. Es wird dabei in einer bestimmten Anzahl von Menschen gezählt, bei wie vielen die Parkinson-Krankheit diagnostiziert wurde, und wie viele spezifische Merkmale aufweisen – also zum Beispiel Raucher sind. Die statistische Analyse zeigt, dass unter Rauchern weniger Menschen an Parkinson erkranken, was heißt, dass Rauchen mit einem geringeren Risiko assoziiert ist. Eine Assoziation ist aber nicht dasselbe wie ein kausaler Zusammenhang. In epidemiologischen Studien werden Raucher nicht über einen längeren Zeitraum beobachtet und es wird nicht erfasst, wie viele von ihnen die Parkinson-Krankheit entwickeln; eine Kausalität ist also nicht erwiesen. Angesichts der bekannten schädlichen Nebenwirkungen des Rauchens wird von Seiten der Medizinwissenschaft dringend davon abgeraten, zum Schutz vor Parkinson zu rauchen.
Gibt es Umweltfaktoren, deren Schädlichkeit als erwiesen gilt?
Mehrere Studien deuten darauf hin, dass ein häufigeres Auftreten der Parkinson-Krankheit mit bestimmten Umweltschadstoffen zusammenhängen könnte; dazu gehören organische Lösungsmittel, die in Klebstoffen sowie Erdöl und seinen Derivaten enthalten sind, toxische Substanzen, wie sie in synthetischen Rauschmitteln vorkommen, und Pestizide. In Frankreich wird Parkinson seit 2012 als landwirtschaftliche Berufskrankheit anerkannt. An der Universität Trient und im Krankenhaus Santa Chiara hat man beobachtet, dass im Nonstal ungewöhnlich viele Frauen an Parkinson erkranken; viele dieser Frauen arbeiten oder arbeiteten in den Apfellagerhallen. Wie im Fall des Rauchens wurde jedoch kein kausaler Zusammenhang nachgewiesen. Vor einigen Jahren untersuchte ein kanadisches Forscherteam die Bevölkerung der landwirtschaftlich geprägten Provinz Saskatchewan, in der viele Menschen von der Krankheit betroffen sind. Die Wissenschaftler vermuteten einen Zusammenhang mit einem bestimmten Pestizid, entdeckten aber schließlich eine für die dortige Bevölkerung charakteristische Genmutation. Auch starke Schläge auf den Kopf, wie zum Beispiel Boxer oder Fußballer sie erleiden, können die Krankheit auslösen.
Was passiert im Gehirn von Parkinson-Kranken?
In beiden Gehirnhälften befindet sich ein winziger, mit bloßem Auge kaum sichtbarer Teil, der wegen der dunklen Farbe seiner Nervenzellen Substantia nigra compacta (kompakte schwarze Substanz) genannt wird. Über lange, verzweigte Fortsätze, sogenannte Axone, kommunizieren die Neuronen der Substantia nigra mit anderen, weiter entfernten Bereichen des Gehirns, insbesondere mit dem Teil des Gehirns, der die willkürlichen Bewegungen steuert. Bei Parkinson-Kranken sterben die Neuronen in der Substantia nigra allmählich ab. Sie kommunizieren nicht mehr mit den anderen Teilen des Gehirns, und die Patienten können ihre Bewegungen nicht mehr steuern – sie sind aber weiterhin in der Lage, unwillkürliche Bewegungen auszuführen. Parkinson-Kranke können zum Beispiel ausweichen, wenn beim Gehen ein Gegenstand vor ihnen auftaucht: Ihr Gehirn erkennt ein Hindernis und hebt instinktiv das Bein. Fällt den gleichen Menschen jedoch ein Gegenstand aus der Hand, sind sie nicht in der Lage, ihn aufzuheben. Im fortgeschrittenen Stadium sind die Kranken in ihrem Körper gefangen und nicht einmal mehr fähig, zu sprechen.
Die Neuronen der Substantia nigra sterben ab. In den überlebenden Neuronen bilden sich kleine Einschlüsse, die sogenannten Lewy-Körperchen. © Eurac Research | Fabio Dalvit
Stirbt man an Parkinson?
Wenn Parkinson-Patienten sterben, dann ist in der allgemeinen Wahrnehmung nicht die Krankheit der Grund, sondern Altersschwäche. Doch obwohl Parkinson nicht mit einer Krebserkrankung vergleichbar ist, die einen viel schnelleren Verlauf und eine höhere und „sichtbarere" Sterblichkeit hat, sterben Menschen tatsächlich an Parkinson: Die Lebenserwartung verringert sich um vier bis elf Jahre, und – ein nicht zu vernachlässigender Aspekt – die Krankheit beeinträchtigt die Lebensqualität stark.
Die Lebenserwartung von Parkinson-Kranken verringert sich um vier bis elf Jahre.
Der Tremor ist das bekannteste Symptom. Was sind andere häufige Symptome?
Das typische Zittern, das wir allgemein am stärksten mit der Parkinson-Krankheit verbinden, ist weder das wichtigste Symptom, noch bedeutet es die größte Beeinträchtigung. Die Ärzte unterscheiden motorische und nicht-motorische Symptome (einige können bis zu 15 Jahre vor den motorischen Symptomen auftreten)
Ist Parkinson heilbar?
Eine Heilung in dem Sinne, dass der Krankheitsprozess angehalten, das Fortschreiten der Erkrankung verhindert wird, gibt es leider nicht. Die Symptome können aber behandelt werden, etwa durch den Wirkstoff L-Dopa, der die motorischen Störungen sehr gut kontrolliert. Die Wirksamkeit der Medikamente lässt jedoch nach einigen Jahren nach, dazu kommen erhebliche Nebenwirkungen. Für die nicht-motorischen Symptome gibt es keine spezifische Behandlung; der Neurologe muss Therapien mit anderen Indikationen einsetzen, etwa Antidepressiva, und sie mit Behandlungsmethoden wie Physiotherapie ergänzen, um die Lebensqualität so weit wie möglich zu erhalten.
Nur die Symptome können behandelt werden – eine Therapie, die die Krankheit aufhält, gibt es bislang nicht.
Gibt es eine Impfung?
Im Moment noch nicht. Einige Ansätze werden derzeit in klinischen Studien getestet, darunter ein Impfstoff, den das österreichische Biotech-Unternehmen Affiris entwickelt. Die Firma hat kürzlich erste Daten veröffentlicht: Die Ergebnisse der vierjährigen Phase-I-Studie (die erste von drei Phasen der klinischen Prüfung) scheinen vielversprechend zu sein.
Wie weit entfernt ist man davon, die Erkrankung heilen zu können?
Wenn Parkinson diagnostiziert wird, hat die Krankheit meist schon großen Schaden angerichtet: Mindestens 50 Prozent der Neuronen in der Substantia nigra gehen zugrunde, bevor sich die typischen Symptome zeigen. Eine heilende Therapie würde also schon mit großer Verspätung einsetzen. Aus diesem Grund konzentriert sich die Forschung auf die Diagnosemethoden: Es geht darum, den Degenerationsprozess der Neuronen so früh wie möglich zu erkennen und aufzuhalten.
Wenn die ersten Symptome auftreten, sind schon mindestens 50 Prozent der Neuronen in der Substantia nigra verloren.
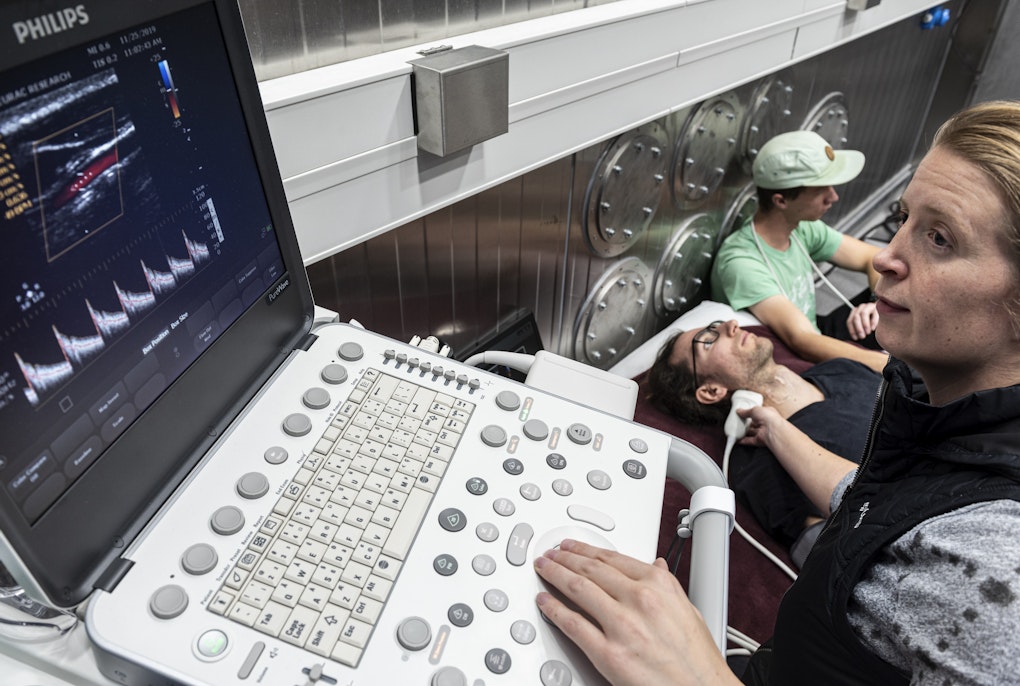
Was könnte einen Durchbruch in der Diagnose bedeuten?
Derzeit erfolgt die Diagnose klinisch, durch neurologische Untersuchungen; definitive Bestätigung bringt erst eine Autopsie: Ist die Substantia nigra nicht mehr dunkel, bedeutet das, die Neuronen sind tatsächlich durch Parkinson abgestorben. Der Durchbruch in der Diagnose wäre ein bildgebendes Verfahren, also eine Technologie, die die Funktion von Organen oder Geweben im menschlichen Körper sehr präzise und detailliert abbilden kann. Die Michael J. Fox Foundation hat zwei Millionen Dollar gestiftet, um Forscher und Forscherinnen zu unterstützen, die Kontrastmittel für das nuklearmedizinische Diagnoseverfahren Positronen-Emissions-Tomografie (PET) erforschen; Ziel ist, frühe Anzeichen der Krankheit im Gehirn sichtbar zu machen, bevor offenkundige Symptome auftreten. Große Bedeutung hat zudem die Grundlagenforschung, um zu verstehen, wo die krankheitsverursachenden Veränderungen in den molekularen Prozessen ihren Ursprung haben.
Die Diagnose bestätigen kann nur eine Autopsie.
Molekulare Forschung bei Eurac Research
Was passiert in den Zellen, wenn man an Parkinson erkrankt? In welcher Reihenfolge treten die Ereignisse ein, und wie hängen sie zusammen? Was bewirken genetische Mutationen? Wie können wir in den Prozess eingreifen? Am Institut für Biomedizin untersuchen Forscherinnen und Forscher aus den Bereichen Biologie, Genetik, Statistik und Pharmazeutische Chemie die molekularen Prozesse, die bei der Parkinson-Krankheit eine Rolle spielen. Ziel ist, herauszufinden, wie man die Krankheit aufhalten oder verlangsamen kann.
Parkin-Gen und Mitochondrien
Parkin ist eines der Gene, die für eine erbliche Form von Parkinson verantwortlich sind: Ist Parkin mutiert und dadurch in seiner Funktion eingeschränkt, dann beeinträchtigt dies die Mitochondrien, die die Zellen mit Energie versorgen. Da Neuronen viel Energie benötigen, kann eine Dysfunktion der Mitochondrien zum Zelltod beitragen. Auf der Suche nach mitochondrialen Eiweißstoffen, die mit Parkin zusammenarbeiten, um die Funktion der Mitochondrien zu erhalten, entdeckten die Forscherinnen von Eurac Research ein Protein namens SLP-2: Können Mitochondrien mit einer Therapie, die auf das SLP-2-Protein wirkt, wieder funktionsfähig gemacht und damit Neuronen gerettet werden? Die Forscherinnen testen dies, indem sie die Konzentration von SLP-2 in verschiedenen Zellmodellen erhöhen. Die ersten Ergebnisse sind positiv.
Für diese Forschung werden induzierte pluripotente Stammzellen verwendet
Als Ausgangsmaterial dienen Haut- oder Blutzellen, die ihrer Eigenschaften beraubt, also in „neutrale“ Stammzellen (sogenannte induzierte pluripotente Stammzellen) verwandelt (reprogrammiert) werden. Anschließend können sie in jeden beliebigen Zelltyp differenziert werden, man kann also Zellen mit verschiedenen Funktionen erhalten. In unserem Fall Neuronen, Gehirnzellen. © Eurac Research | Fabio Dalvit
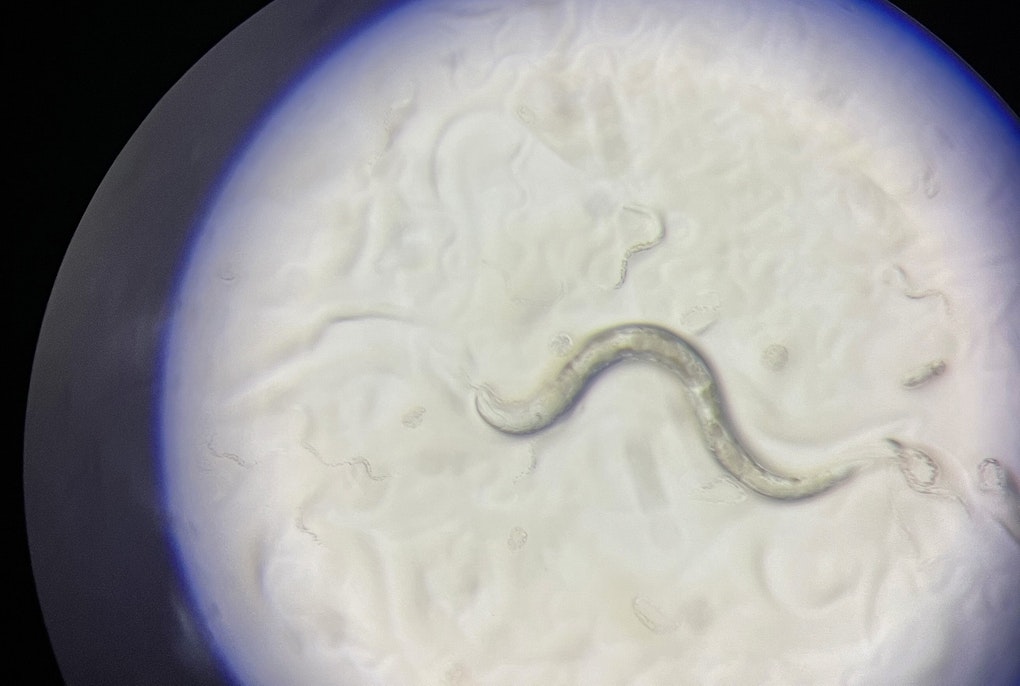
Mikroskopische Aufnahmen: Neuronen, die im Labor aus induzierten pluripotenten Stammzellen (iPSCs) gewonnen werden. Um die Mitochondrien, die Energielieferanten der Zelle, sichtbar zu machen und ihre Rolle in der Parkinson-Erkrankung zu untersuchen, werden sie mit chemischen Reagenzien angefärbt.
In Blau die Zellkerne, in Grün die Mitochondrien und in Rot das mitochondriale Protein SLP-2
Die Mitochondrien sind nicht statische Elemente in den Zellen, im Gegenteil, sie teilen sich und verschmelzen kontinuierlich. Eine Zeitraffer-Aufnahme, die vier Stunden abdeckt
LRRK2-Gen und Lewy-Körperchen
Menschliche Zellen bauen Teile ihrer selbst ab, um Abfallstoffe zu entsorgen oder weil sie Nährstoffe brauchen. Dieser Prozess wird Autophagie genannt; es ist der gleiche Mechanismus, durch den wir „Fett verbrennen", wenn wir fasten. Bei Parkinson-Kranken mit einer Mutation im LRRK2-Gen funktioniert die Autophagie nicht richtig. In den Neuronen kommt es deshalb zur Anhäufung des Proteins Alpha-Synuclein, die die Zellen vergiften (Alpha-Synuclein ist ein Hauptbestandteil der Lewy-Körperchen). Eine Forschergruppe von Eurac Research hat in Zusammenarbeit mit dem Team von Martin Lévesque von der Universität Laval (Kanada) Zellmodelle verwendet, um die Wirkung des LRRK2-Gens zu verändern und so die Autophagie wiederherzustellen; sie haben nachgewiesen, dass die Lewy-Körperchen sich tatsächlich reduzieren. Die Forscher und Forscherinnen sehen darin eine vielversprechende neue Strategie zur Bekämpfung der Krankheit.
Die Immunfluoreszenz ist eine hochentwickelte Technik, die es ermöglicht, die Vorgänge innerhalb der Zellen genauer zu untersuchen. Diese Bilder zeigen Zellmodelle von Neuronen in Kultur. Dank solcher Aufnahmen kann das Forschungsteam beobachten, wie die Neuronen kommunizieren (oder nicht kommunizieren) und wie sie Abfallstoffe entsorgen.
LRRK2-Gen und die Kommunikation zwischen Neuronen
Wo beginnt die Parkinson-Krankheit? Nach neuesten Studien betreffen die ersten Veränderungen die Kommunikation zwischen den Neuronen. Ein Forschungsschwerpunkt bei Eurac Research ist genau diese Kommunikation: Die Signalübertragung an den Synapsen am Ende der Axone, also jener Bahnen, über die die Neuronen Informationen und Anweisungen an andere Gehirnregionen übertragen.
Mikrotubuläre Struktur
So nennt man die Proteinstruktur, die die Neuronen „zusammenhält". In Zusammenarbeit mit der Universität Mailand untersucht ein Team von Eurac Research diese Strukturen und versucht zu verstehen, ob und wie Anhäufungen von Alpha-Synuclein auch sie beschädigen.
Wie viele öffentliche und private Mittel fließen in die Parkinson-Forschung?
Im Vergleich zu anderen Krankheiten wird in die Erforschung von Parkinson nicht viel Geld investiert (das US-Gesundheitsministerium zum Beispiel gab im Jahr 2019 rund 240 Millionen Dollar für die Parkinson-Forschung aus, verglichen mit eineinhalb Milliarden für die Alzheimer-Forschung). Die Erforschung neurodegenerativer Erkrankungen befindet sich in einer schwierigen Phase, weil große Unternehmen sich etwas daraus zurückgezogen haben. Der Grund: Neuroprotektive Therapien zu testen ist sehr teuer, und das Risiko, dass sie in der klinischen Erprobung durchfallen und nie vermarktet werden, ist hoch. Es gibt private Organisationen, die speziell Parkinson-Forschung finanzieren, wie die Michael J. Fox Foundation und die Parkinson Disease Foundation in den USA, Parkinson's UK, die Parkinson Association Canada und das Weston Brain Institute in Kanada sowie in geringerem Umfang die Fritz Thyssen Stiftung in Deutschland und Telethon in Italien. Bei Regierungsbehörden oder öffentlichen Einrichtungen konkurrieren Forschungsgruppen um die generell für Forschung vorgesehenen Mittel. Südtirol ist in Partnerschaftsprogramme mit deutschen, österreichischen, luxemburgischen und schweizerischen Regierungsstellen sowie mit dem Euregio-Wissenschaftsfonds eingebunden. Fördermittel zu finden und wettbewerbsfähige Anträge vorzubereiten, ist ein zentraler Teil der Arbeit von Forschungsteams, der viel Zeit und Energie in Anspruch nimmt.
Die großen Pharma-Unternehmen haben sich etwas aus der Forschung zu neurodegenerativen Erkrankungen zurückgezogen: Studien kosten sehr viel, und das Risiko, nicht zu marktfähigen Therapien zu kommen, ist hoch.
Was sind die wichtigsten Anlaufstellen für Kranke in Südtirol?
Zum einen die Parkinson-Ambulanzen der Krankenhäuser. Außerdem vereint die Südtiroler Gesellschaft für Parkinson und verwandte Erkrankungen verschiedene Selbsthilfegruppen.
eurac e+learning

Der digitale Kurs speziell für Oberschulen zum Thema Parkinson ist kostenfrei online unter https://e-learning.eurac.edu/de abrufbar. Viel Spaß beim Lernen!
 Science that inspire
Science that inspireWissenschaftliche Publikationen
Eine laufend aktualisierte Liste der Publikationen von Eurac Research zu diesem Thema ist im Institutionellen Archiv Bozen verfügbar.
Publikationen von Irene Pichler und Mattia Volta finden Sie auf ihren ORCID Seiten: Irene Pichler, Mattia Volta.
Impressum
Irene Pichler und Mattia Volta, Institut für Biomedizin, Eurac Research
Mit Unterstützung von Alessandra Zanon
Redaktion: Valentina Bergonzi
Übersetzung: Barbara Baumgartner
Illustrationen: Oscar Diodoro
Videoanimationen: Fabio Dalvit
Bildredaktion: Annelie Bortolotti, Thomas Iacopino, Matthias Mühlberger
Grafik: Elisabeth Aster