magazine_ Article
Was Rauchen mit unserer Mundflora macht
Eine Studie zeigt den Effekt des Zigarettenkonsums – und des Aufhörens
Im Rahmen der CHRIS-Studie ging ein Forschungsteam der Frage nach, wie sich Rauchen auf die Bakteriengemeinschaft in unserem Mund auswirkt. Sehr deutlich, so das Ergebnis der Untersuchung, die weltweit eine der größten zum Speichelmikrobiom ist. Mit zunehmendem Zigarettenkonsum verringert sich die Zahl der Bakterien, die Sauerstoff brauchen. Und wer aufhört, ist erst fünf Jahre später nicht mehr von jemandem zu unterscheiden, der nie angefangen hat.
Der Vater des Biotechnologen Giacomo Antonello, ein Zahnarzt, verblüffte Patienten manchmal mit seinen nahezu hellseherisch scheinenden diagnostischen Fähigkeiten: Ein Blick in ihren Mund – und er riet, einen Facharzt aufzusuchen, denn womöglich hätten sie ein Problem am Herzen; was sich dann auch öfters als richtig herausstellte. Die Betroffenen waren immer sehr beeindruckt. Für Fachleute sind solche Treffer weniger überraschend: Empirische Studien belegen, dass zwischen Parodontitis und verschiedenen Herz-Kreislauf-Erkrankungen tatsächlich häufig ein Zusammenhang besteht, wenn auch die genauen Mechanismen nicht restlich geklärt sind. Antonello, der derzeit für seinen PhD am Institut für Biomedizin forscht, hat nun mit Kollegen am Institut für Biomedizin von Eurac Research gerade eine Studie abgeschlossen, die auf einen möglichen Faktor hinweist: Bei Menschen, die rauchen, könnten die Veränderungen im Mundmikrobiom zum erhöhten Risiko für diese Erkrankungen beitragen.
Vor allem aber beantwortet die Untersuchung, die im Rahmen der CHRIS-Studie im Vinschgau durchgeführt wurde, zwei zentrale Fragen: Was genau passiert mit der Bakteriengemeinschaft im Mund, dem sogenannten oralen Mikrobiom, wenn wir rauchen? Und welche Wirkung hat es, wenn wir das Rauchen aufgeben? Um das herauszufinden, analysierte das Forschungsteam in Bozen gemeinsam mit der Epidemiologin Betsy Foxman von der Universität Michigan Speichelproben von mehr als 1600 Menschen. Mit dieser Probandenzahl ist die Studie für das Forschungsfeld „riesig“, wie der Bioinformatiker Christian Fuchsberger unterstreicht, der Antonello als Doktorvater zur Seite steht: „Zum Speichelmikrobiom gibt es kaum große Studien: Das ist ein junges Forschungsgebiet, in dem sich gerade sehr viel tut – aber manches auch nicht sauber gemacht wird; viele Studien arbeiten beispielsweise mit sehr geringen Fallzahlen, die Ergebnisse sind dann nicht generalisierbar.“
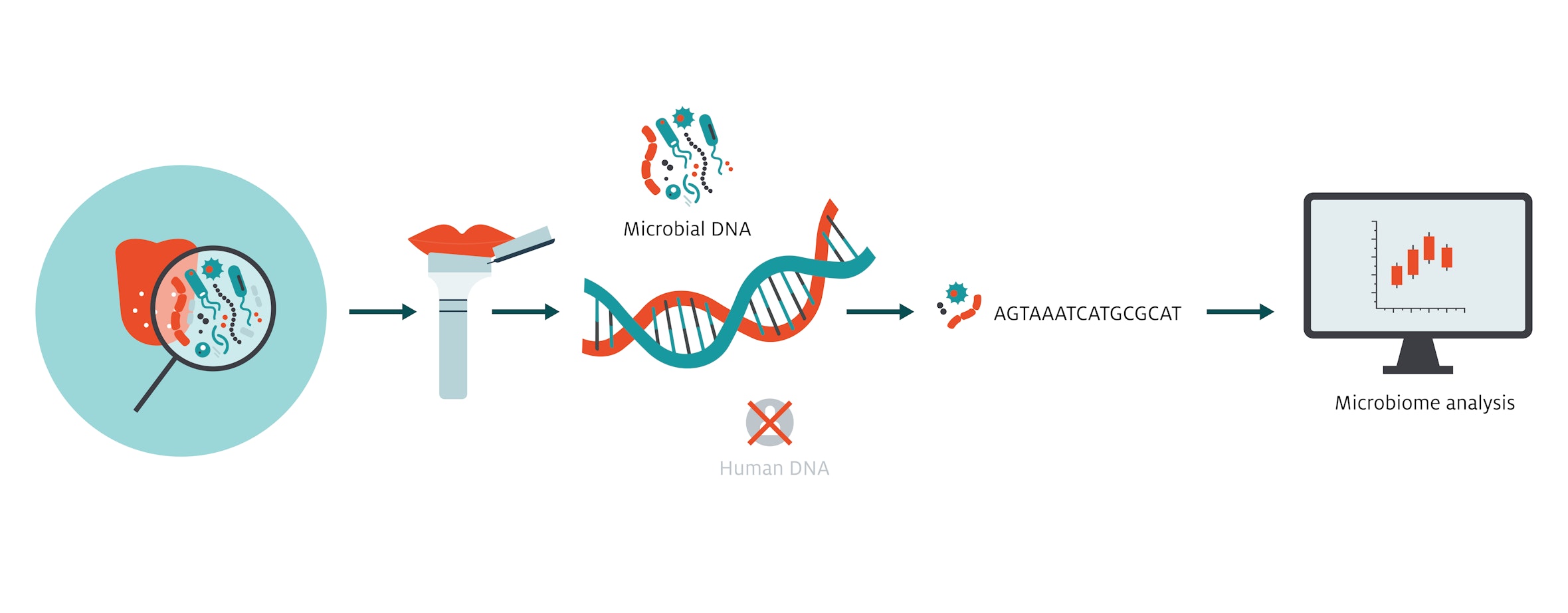 Photo: Silke De Vivo | Eurac Research
Photo: Silke De Vivo | Eurac ResearchDie gesamte Mikrobiomforschung ist ein ziemlich junges Gebiet: Noch vor ein paar Jahrzehnten wurde die Gemeinschaft der Billionen Mikroorganismen, die auf und im Menschen leben – die meisten im Verdauungstrakt – von der Wissenschaft eher als ein Nebenschauplatz betrachtet. Jetzt steht dieses Mikrobiom im Zentrum des Interesses, denn man hat erkannt, dass es für unsere Entwicklung und Gesundheit große Bedeutung hat. Vor allem das Darmmikrobiom wird intensiv erforscht; auch am Institut für Biomedizin läuft dazu gerade eine große Studie (siehe Box). Im Vergleich zur Mikrobendichte des Darms, wo tausende Stämme unterschiedlicher Bakterien leben, ist unser Mund nur dünn besiedelt. Für Untersuchungen hat Speichel aber einen besonderen Vorteil: Proben zu erhalten ist außerordentlich einfach. Gelänge es, in der Mundflora Veränderungen zu identifizieren, die zuverlässig auf bestimmte Erkrankungen hindeuten (Biomarker), wäre dies ein wertvolles, für Gesundheitssysteme leicht zu handhabendes diagnostisches Instrument.
Für die Speicheluntersuchung im Rahmen der CHRIS-Studie musste jeder Proband fünf Milliliter in ein Röhrchen spucken. Die Teilnehmenden wurden in Gruppen eingeteilt, je nachdem, ob sie aktuell rauchten, zu rauchen aufgehört, oder nie damit begonnen hatten. Wer aufgehört hatte, wurde nach dem Zeitpunkt der letzten Zigarette gefragt, wer noch rauchte, nach der Zahl der täglichen Zigaretten. Um ein Bild der Mikrobengemeinschaft in jedem Mund zu erhalten – welche Arten mit welcher Häufigkeit vertreten waren – verwendete das Forschungsteam eine universell eingesetzte Technologie zur Identifikation von Bakterien, die Sequenzanalyse des 16S-rRNA-Gens (dieses Gen stellt so etwas wie eine „Identitätskarte“ der verschiedenen Arten dar).
Die Effekte des Rauchens, die wir beobachtet haben, bleiben über Jahre bestehen. Da ist die Frage interessant, ob das in Zusammenhang mit bestimmten Krankheiten steht.
Christian Fuchsberger
Die Auswertung ergab klare Resultate. Wer nie geraucht hat, trägt eine deutlich andere Mikroben-WG im Mund als Menschen, die noch rauchen oder es vor kurzem aufgegeben haben. Der Zigarettenkonsum wirkt sich vor allem auf jene Bakterien aus, die Sauerstoff brauchen: Ihre Zahl nimmt kontinuierlich ab, je mehr Zigaretten man täglich raucht; lässt man das Rauchen sein, nehmen diese aeroben Bakterien nach und nach wieder zu – je länger die rauchfreie Zeit, desto mehr von ihnen finden sich wieder im Speichel. Erst fünf Jahre nach der letzten Zigarette sind ehemalige Raucherinnen und Raucher an ihrem Mundmikrobiom nicht mehr von Menschen zu unterscheiden, die nie geraucht haben. „Die Effekte des Rauchens, die wir beobachtet haben, bleiben also über Jahre bestehen“, sagt Fuchsberger. „Da ist dann natürlich die Frage interessant, ob das in Zusammenhang mit bestimmten Krankheiten steht.“
Raucher haben bekannterweise ein erhöhtes Risiko sowohl für Parodontitis als auch für Herz-Kreislauf-Erkrankungen. Könnten die Veränderungen im Mundmikrobiom, die der Zigarettenkonsum verursacht, dabei eine Rolle spielen? Hier kommt eine Funktion der im Mund lebenden Bakterien ins Spiel, die wie alles was mit unseren Mikrobiom zu tun hat, seit einiger Zeit zunehmend Beachtung findet: Einige dieser Bakterien, hauptsächlich aerobe, verwandeln das Nitrat, das wir mit dem Essen aufnehmen, in Nitrit, aus dem dann Stickstoffmonoxid wird – ein Stoff, der unter anderem für die Regulierung des Blutdrucks wichtig ist. Ist zu wenig Stickstoffmonoxid verfügbar, könnte dies zu schlecht durchblutetem Zahnfleisch und zu Herz-Kreislauf-Erkrankungen beitragen. Nun hat die Studie im Vinschgau zwar nicht das Stickstoffmonoxid im Speichel gemessen, sondern die Mikroben darin untersucht; alles, was das Forschungsteam sagen kann, ist deshalb: Je mehr die Probanden rauchten, desto weniger nitrat-reduzierende Bakterien lebten in ihrem Mund. Dass dies eine zusätzliche Erklärung dafür sein könnte, warum Raucher ein höheres Risiko für Parodontose und Herz-Kreislauf-Erkrankungen haben, ist „eine Hypothese, die in weiteren Studien getestet werden muss“, betont Antonello. Er geht anhand der CHRIS-Proben schon der nächsten Frage nach: Welche Faktoren haben in welchem Ausmaß Einfluss auf unsere Mundflora? Welche Rolle spielt die Genetik, welche die Menschen, mit denen wir im gleichen Haushalt leben? Antwort darauf wird er erst in etwa einem Jahr geben können, aber eines zeichnet sich schon jetzt sehr deutlich ab: Mit wem wir zusammenleben, hat auch hierfür große Bedeutung.
Mikrobiomforschung im Rahmen der CHRIS-Studie
Wie sich Rauchen auf die Zusammensetzung der Bakteriengemeinschaft in unserem Mund auswirkt, und mit welchen möglichen Folgen für unsere Gesundheit, ist nicht die einzige Forschungsfrage zum Mikrobiom, der Wissenschaftlerteams anhand der Daten der CHRIS-Studie nachgehen. Eine andere große Studie untersucht die Rolle der Darmflora bei Typ-2-Diabetes und Fettlebererkrankung, die nicht auf übermäßigen Alkoholkonsum zurückzuführen ist (NAFLD – non-alcoholic fatty liver disease). Belegt ist, dass beide Krankheiten mit einer veränderten Zusammensetzung der Mikrobengemeinschaft im Darm einhergehen; die genauen Zusammenhänge sind jedoch noch unklar. Um sie besser zu verstehen, wurden rund 350 Teilnehmende der CHRIS-Studie – die Hälfte davon an Typ-2-Diabetes erkrankt – gebeten, an weiteren Untersuchungen teilzunehmen; unter anderem wurde an den Probanden eine Ultraschalluntersuchung der Leber durchgeführt; außerdem wurden Stuhl- und Speichelproben für die Untersuchung des Mikrobioms genommen. Die Ergebnisse der Studie, bei der das Forschungsteam mit den weltweit anerkannten Mikrobiom-Experten Nicola Segata von der Universität Trient und Herbert Tilg von der Medizinischen Universität Innsbruck zusammenarbeiten, werden für 2024 erwartet.